 A molekulák közötti kapcsolatot létrehozó viszonylag gyengébb (általában az atomokat összetartó erőknél nagyságrenddel kisebb) erők.
A molekulák közötti kapcsolatot létrehozó viszonylag gyengébb (általában az atomokat összetartó erőknél nagyságrenddel kisebb) erők.Van der Waals-erők
(intermolekuláris erők, másodrendű kötések, dipólus-dipólus kölcsönhatás, indukciós erők, dipólus-indukált dipólus erők, diszperziós erők, London erők)
 A molekulák közötti kapcsolatot létrehozó viszonylag gyengébb (általában az atomokat összetartó erőknél nagyságrenddel kisebb) erők.
A molekulák közötti kapcsolatot létrehozó viszonylag gyengébb (általában az atomokat összetartó erőknél nagyságrenddel kisebb) erők.
Az intermolekuláris erők (Van der Waals-erők) fő típusai:
Dipólus-dipólus kölcsönhatás
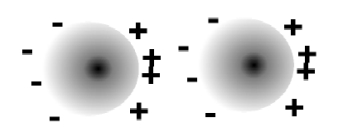
Poláris molekulák között az állandó dipólusmomentum miatt jön létre , ahol a pozitív pólus a másik molekula negatív pólusát vonzza.
Indukciós (dipólus-indukált dipólus) erők
Egy poláris molekula a közelében lévő apoláris molekula elektronfelhőjét eltorzítja (polarizálja), így időlegesen dipólust indukál benne.
Diszperziós (London) erők
Apoláris molekulák és nemesgázok között ható, a leggyengébb, de univerzális erő. Az elektronok mozgása miatti pillanatnyi dipólusok hozzák létre.
Hidrogénkötés
A dipólus-dipólus kölcsönhatás egy speciális, erős fajtája.
A Van der Waals-féle erők úgy jönnek létre, hogy az elektromos szempontból telített molekulákban lévő atomok pozitív magjai és negatív elektronjai között, még bizonyos, a töltési-súlypontok helyzetbeli különbségei által kiváltott vonzási erők (dipóluserők) indulnak ki a szomszédos molekulák atomjainak elektronhéjai irányába. Ebben az esetben tehát úgynevezett intermolekuláris erőkről van szó.
A Van der Waals-féle erők egyaránt hatnak gázhalmazállapotú, folyékony és szilárd anyagok molekulái között. A csepfolyósított és megfagyasztott nemesgázok atomjait például csak a Van der Waals-féle erők tartják össze, minthogy a komplett elektronhéjak (oktett) létezése következtében kémiai természetű vonzóerőkről nem lehet szó.
Ezek az erők a felelősek a van der Waals egyenletben az A/V2 kifejezésért.
Ezek az erők, okozzák a gázok ideálistól eltérő viselkedését és a molekularácsos kristályok rácsenergiáját.