 Előfordulás
ElőfordulásA természetben a manganozit nevű ásványként (a képen) megtalálható.
mangán-oxidok
(mangán(II)-oxid, mangán-monoxid, manganozit, mangán(III)-oxid, Bixbyit, trimangán-tetraoxid, manganomangán-oxid, mangán-heptoxid)
- Mangán(II)-oxid, mangán-monoxid (MnO), a két vegyértékű mangán oxidja.
 Előfordulás
Előfordulás
A természetben a manganozit nevű ásványként
(a képen) megtalálható.
Előállítás
Mangán(II)-karbonát hevítésével keletkezik, szürkészöld vízoldhatatlan por
alakjában.
Fizikai és kémiai tulajdonságai
Zöldesfekete kristályos
anyag.
Sűrűség: 5,45 g/cm3
Olvadáspontja
1650°C
Vízben nem oldódik.
- Mangán(III)-oxid, (Mn2O3), a három vegyértékű mangán oxidja.
 Előfordulás
Előfordulás
A természetben a Bixbyit nevű ásványként
(a képen) megtalálható.
Fizikai és kémiai tulajdonságai
Zöldesfekete kristályos
anyag.
Sűrűség: 5,45 g/cm3
Olvadáspontja
1650°C
Vízben nem oldódik.
Sósavval klórt fejleszt.
- Mangán-dioxid, barnakő (külön címszóban megtalálható).
- Trimangán-tetraoxid, manganomangán-oxid (Mn3O4), a mangán egyik oxidja.
Fizikai és kémiai tulajdonságai
Barnás fekete kristályos
por.
Sűrűség: 4,5 g/cm3
Olvadáspontja 940°C
Vízben nem oldódik.
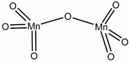 - Mangán-heptoxid (Mn2O7), a hét vegyértékű
mangán oxidja.
- Mangán-heptoxid (Mn2O7), a hét vegyértékű
mangán oxidja.
Előállítás
Kálium-permanganátból tömény kénsavval keletkezik:
Fizikai és kémiai tulajdonságai
Sötétvörös, olajszerű folyadék.
Szilárd állapotban vörös színű, monoklin kristályokból áll.
Sűrűség: 2,79 g/cm3
Olvadáspontja 5,9°C
Nagyon erős oxidálószer. Melegítve viharosan oxigént fejleszt, sőt robban.
Vízzel permangánsavat ad.