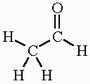
 C2H4O
C2H4OAz aldehidek homológ sorának második tagja.
acetaldehid
(etanal, Wacker-eljárás, paraldehid, metaldehid)
 C2H4O
C2H4O
Az aldehidek homológ
sorának második tagja.
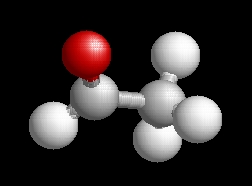
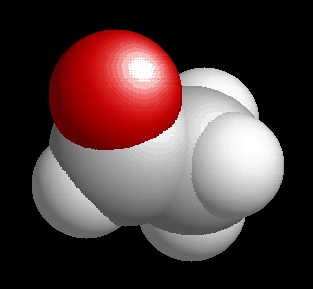
Az acetaldehid molekulaképe balra golyó és pálcika jobbra térkitöltéses megjelenítésben.
|
|
Az Acetald.pdb koordináta fájl térben megjeleníthető a https://sourceforge.net/projects/openrasmol/ címről letölthető molekulamegjelenítő programmal.
Előfordulás
Etilalkohol oxidációjakor
keletkezik, így megtalálható az alkoholos erjedés
termékei közt is kis mennyiségben. Megtalálható érett gyümölcsökben, kávéban,
friss kenyérben.
Előállítás
Etanolból krómsavval (dikromát + kénsav).
Folyékony fázisban, vagy levegővel
fémkatalizátorok
felületén gőzfázisban
oxidálják.
Ma azonban elsősorban acetilénből állítják
elő a Wacker-eljárással.
Ennél az eljárásnál az acetilén és
a levegő keverékét
palládium(II)-kloridot és réz(II)-kloridot tartalmazó oldaton vezetik keresztül.
A Pd2+-ionok komplexet képeznek az eténnel, így a C=C kötés
pi-elektronjai fogékonnyá válnak a vízmolekulák nukleofil támadására.
A keletkezett komplex
acetaldehidre és fém palládiumra bomlik. A Cu2+-ion oxidálja
vissza a palládiumot Pd2+-á és redukálódik Cu+-ionná. A jelenlévő levegő oxidálja
vissza a Cu+-iont Cu2+-ionná.
Az eljárás Alexander von Wacker (1846-1922) után nevezték el.
 Fizikai és kémiai tulajdonságai
Fizikai és kémiai tulajdonságai
Szúrós szagú, szintelen, mozgékony folyadék.
Olvadáspont: -123°C
Forráspont: 20.2°C
Sűrűség: 0,78
Vízben jól oldódik.
Könnyen polimerizálódik,
ekkor paraldehid (trimer)
keletkezik belőle hőfejlődés
közben.
A paraldehid folyékony, egy másik polimere
a metaldehid /C4O4H4(CH3)4/ szilárd. Ezek a polimerek
már nem redukálnak,
tehát szabad aldehidgyököt
nem tartalmaznak, hanem gyűrűs
szerkezetűek.
Felhasználás
Fontos vegyipari alapanyag.
Oldószerként is használják.
A metaldehidet szilárd fűtőanyagként
használják.
Biológia
A szervezetben is acetaldehiddé oxidálódik
első lépésben az etilalkohol.