termokémia
(exoterm, endoterm)
A kémiai reakciókat kísérő energiaváltozásokat
vizsgáló tudományág.
A kémiai reakciók során felszabadulhat
és elnyelődhet hő- (villamos-,
fény- stb.) energia.
A kémiai reakciók során a reakcióegyenlettel
kifejezett kémiai változás mellett a reagáló rendszer és a környezet között
kölcsönhatások léphetnek fel. Ezek
közül legáltalánosabb a reagáló rendszer környezetére kifejzett hőleadás
vagy hőfelvétel.
Minden reakció valamilyen hőhatással
jár.
Ha kémiai folyamatban hő
szabadul fel, exoterm, folyamatról beszélünk.
Ilyenek például az égési folyamatok, sav-bázis
reakciók.
Ha hő használódik fel, endoterm
folyamatról beszélünk.
Ilyen például a sók oldódása.
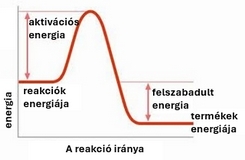
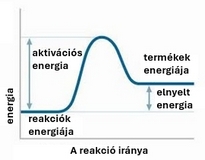
Az alábbi ábrákon a reakciók mechanizmusa és egy-egy példa látható.
|
exoterm reakció.
|
endoterm reakció.
|
 |
 |
 |
 |
A hőmérséklet változás nélkül felszabaduló
vagy eltűnő hőt látens (rejtett) hőnek
nevezik.
Előfordul olvadásnál és fagyásnál,
párolgásnál és lecsapódásnál,
valamint gázállapotból szilárd
állapotba történő átmenetnél és szublimációnál,
oldódásnál és kristályosodásnál,
illetve módosulatváltozásnál (pl. a
rombos kén monoklin
kénné történő átalakulásakor).
A fizikai kémiai folyamatoknál előforduló hőmennyiségek:
oldódáshő, olvadáshő,
párolgáshő, égéshő, képződéshő, közömbösítési hő
Termokémiai módszerek használatosak pl. az élelmiszerek energiatartalmának
meghatározásánál is.