Joule törvénye
Egy adott tömegű gáz
belső energiája független a térfogatától
és nyomásától, csak a hőmérséklet
függvénye.
Ez a törvény, amelyet James Prescott Joule
fogalmazott meg, csak ideális gázokra
érvényes (amelyre megadja a termodinamikai
hőmérséklet definícióját), mivel reális
gázokban a molekulák közti erők
változást hoznak létre a belső energiában,
térfogatváltozást okozva. Lásd Joule-Thomson-hatás.
A Joule törvény differenciális alakját egy homogén drótban leadott teljesítmény (P) és a drót térfogatának (V) hányadosa adja meg:
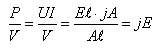
Differenciális formája:
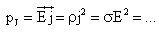
ahol pj az egységnyi térfogatban egységnyi idő alatt keletkezett hő, vagyis a Joule-hő teljesítménysűrűsége.