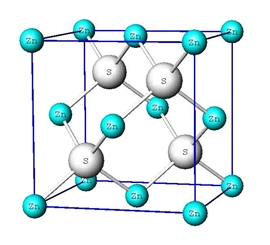

atomrács
Sokkal kevésbé gyakoriak, mint az ionrácsok. Ilyen rácsa van pl. a cink-szulfidnak (ZnS) (lásd a képeken), bór-nitridnek (BN), stb.
 |
 |
|---|
Az atomokat úgynevezett kovalens
kötés tartja össze, amely ugyan végső elemzésben ugyanolyan elektrosztatikus
megosztás eredetű, mint az ionok közti
kötés, de irányított.
A szénatom négy vegyértéke
például a tetraéder négy csúcsa felé irányul a középpontból, tehát bármely két
vegyérték tehát 109°28' szöget
zár be egymással.
Atomrácsokban egyes önálló molekulák
nem ismerhetők fel, hanem végtelen kiterjedésű, egy-, két-, vagy háromdimenziós
térbeli alakzatokat alkotnak.
Az atomvegyületek sokszor sötét színüek, ha mégis átlátszóak akkor törésmutatójuk
2 fölötti.
Olvadáspontjuk és forráspontjuk
magas, a kettő különbsége is nagy.
Oldhatóságuk minimális, a töltés
nélküli atomok nem hidratálódnak.