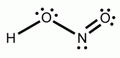 HNO2
HNO2Középerős, egybázisú sav.
salétromossav
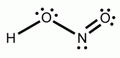 HNO2
HNO2
Középerős, egybázisú sav.
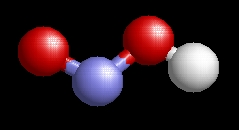
A salétromossav molekulaképe balra golyó és pálcika jobbra térkitöltéses megjelenítésben.
|

|
A hno2.pdb koordináta fájl térben megjeleníthető a https://sourceforge.net/projects/openrasmol/ címről letölthető molekulamegjelenítő programmal
Előfordulás
Kis mennyiségben a természetben is előfordul, de főleg sói
találhatók.
A légkörben is előfordul
nitrogén-trioxid vízzel
történő reakciója (lásd lentebb) miatt, savas
eső egyik okozója.
Előállítás
Sóiból kénsavval oldata előállítható, de legfeljebb 0,5n töménységben és csak
nagyon hidegen.
A nitrogén-trioxid vízzel
salétromossavvá egyesül:
N2O3 + H2O -> 2 HNO2
Fizikai és kémiai tulajdonságok
Oldata halványkék színű.
Bomlékony
3HNO2 -> HNO3 + 2NO + H2O (diszproporcionálódás)
Oxidáló hatású, például a jodidiont
(I-), kénhidrogént (H2S) oxidálja, miközben nitrogén-oxiddá
(NO) redukálódik.
Néha redukáló hatású, például a kálium-permanganát savanyú oldatát mangán(II)-szulfáttá
redukálja, miközben salétromsavvá oxidálódik.
Sói a nitritek.
Anhidridje a nitrogén-trioxid (N2O3).
Felhasználás
Diazóniumsók előállítására.
Használják a mérgező és potenciálisan robbanékony nátrium-azid oldat megsemmisítésére.