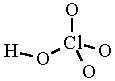
 HClO4
HClO4
A klór egyik oxisava.
perklórsav
(klór(VII)sav)
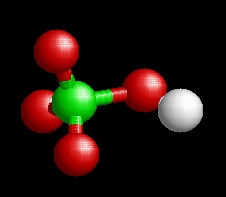
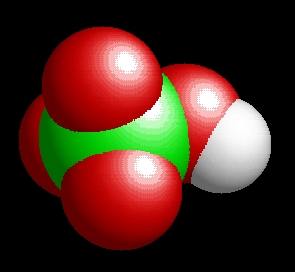
A perklórsav molekulaképe balra golyó és pálcika jobbra térkitöltéses megjelenítésben.
|
|
A hclo4.pdb koordináta fájl térben megjeleníthető a https://sourceforge.net/projects/openrasmol/ címről letölthető molekulamegjelenítő programmal
Előállítás
Laboratóriumban kálium-perklorátból tömény kénsavval
állítható elő:
KClO4 + H2SO4 -> NaHSO4 + HClO4
Vákuumdesztillációval tisztítható.
Fizikai és kémiai tulajdonságai
Tiszta állapotban nem stabil, olajszerű folyadék.
Sűrűsége 1,76 g/cm3 (monohidrát 1,77 g/cm3, dihidrát 1,65 g/cm3)
Olvadáspontja -112°C (monohidrát 48°C, dihidrát 17,8°C)
Forráspontja 39°C ( dihidrát 200°C)
Igen erős, egybázisú sav.
Erős oxidálószer.
Közönséges hőmérsékleten a fémek nem redukálják, hanem hidrogénfejlődés közben
reagálnak vele.
A vízmentes sav lassan bomlik és robbanékony (atmoszférikus nyomáson körülbelül 90°C-on, a monohidrát 110°C-on robban).
Szerves anyagokat meggyújthat.
Oldata higroszkópos tulajdonságú, a levegő nedvessége felhigítja.
Sói a perklorátok,
stabilak, vízben oldódnak.
Felhasználás
Sóit oxidálószerként
használják, pl. pirotechnikai keverékekben.
Széles körben használják szerves anyagok analízis előtti roncsolására, például nehézfém analízisre kerülő állati vagy növényi mintáknál.