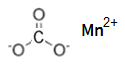 MnCO3
MnCO3A két vegyértékű mangán karbonátja.
mangán(II)-karbonát
(rodokrozit)
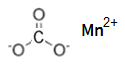 MnCO3
MnCO3
A két vegyértékű
mangán karbonátja.
 Előfordulás
Előfordulás
A természetben nagy tömegben megtalálható a rodokrozit nevű ásvány
formájában (a képen).
(Elnevezése a görög rodokroosz /=rózsaszínű/ szóból ered.)
Hazánkban a Mátrában és a Börzsönyben fordul elő. Szebb kritályait
ékszerként is használják.
Előállítás
Mangán(II) sók
oldatából alkálifémek
karbonátjaival mangán(II)-karbonát
csapadékot adnak (pl.):
MnCl2 + K2CO3 -> MnCO3 + 2 KCl
Fizikai és kémiai tulajdonságai
Barnás, rózsaszínű kristályokból
álló só
Sűrűség: 3,125 g/cm3
Vízben nem oldódik
Hevítve 200°C-on elbomlik:
MnCO3 -> MnO + CO2
Felhasználás
Mangán-dioxid előállítására (az előbbi bomlási reakcióval).
Kerámiák és zománcok színezésére.
Műtrágyaként növények
mangánpótlásra.