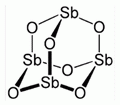
 Sb2O3
Sb2O3antimon(III)-oxid, fehér antimon, antimon-szeszkvioxid, antimonvirág
Az antimon oxidja.
antimon-trioxid
(sénarmontit, valentinit, antimon(III)-oxid, fehér antimon, antimonfehér, antimon-szeszkvioxid, antimonvirág)
 Sb2O3
Sb2O3
antimon(III)-oxid, fehér antimon,
antimon-szeszkvioxid, antimonvirág
Az antimon oxidja.

 Előfordulás
Előfordulás
Ásványként is megtalálható,
mint sénarmontit (a baloldali képen), köbös
kristályszerkezettel, illetve mint valentinit (a jobboldali képen),
rombos kristályszerkezettel.
Előállítás
Antimon elégetésekor,
illetve antimon-halogenidek hidrolízisekor keletkezik.
Fizikai és kémiai tulajdonságok
Fehér kristályos
por.
Gőze Sb4O6
molekulákból áll.
Sűrűsége 5,2-5,7
g/cm3 (a szerkezettől függően)
Olvadáspontja 656°C .
Forráspontja 1550°C (részben szublimál)
ponja 193°C
Vízben nem oldódik.
Hidrogén-fluoridban és sósavban oldódik.
Lúgok is oldják antimonitok keletkezésével:
Sb2O3 + 2 NaOH = 2 NaSbO2 + H2O
Perklórsavval antimon-perklorát (SbO.ClO4)
keletkezik belőle; az antimon (SbO+)
kationként viselkedik.
Hevitésre bomlik.
 Felhasználás
Felhasználás
Textilek, polimerek és bevonatok lángmentesítésére.
Az üveg- és kerámiagyártásban.
A festékgyártásban
pigmentként (antimonfehér).
A PET gyártásnál katalizátorként.
Biológia
Irritálja a nyálkahártyákat.
Hosszabb idő alatt bőrgyulladást okozhat és hatással lehet a tüdőre.