 Ha 1
gramm szén (jele C) atomjai égés közben a levegő oxigén atomjaival szén-dioxid
(CO2) molekulákká egyesülnek, akkor 8 kilogrammkalória, kb. 3400 méterkilogrammsúly
munkavégző képesség szabadul fel
Ha 1
gramm szén (jele C) atomjai égés közben a levegő oxigén atomjaival szén-dioxid
(CO2) molekulákká egyesülnek, akkor 8 kilogrammkalória, kb. 3400 méterkilogrammsúly
munkavégző képesség szabadul felHogyan keletkezik égéskor a meleg?
Még nem feleltünk arra a kérdésre: hogyan tudjuk rábírni a molekulákat
arra, hogy sebesebben mozogjanak? Például ha gyufát gyújtunk, miért keletkezik
láng? Mi lángol abban a lángban? Mi a tűz, a láng egyáltalában? Ez a láng miért
csak meghatározott nagyságú? Hogyan fejlődik a meleg az égéskor?
A hő a molekulák mozgása. Mennél forróbb a levegő, annál sebesebben mozognak
legapróbb részecskéi. Ez világos, tiszta dolog. Azt is tudjuk, hagy az égés
az anyagok atomjainak egyesülése az oxigénatommal.
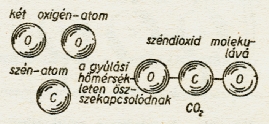
Például a szén égésekor
a szénatom magához kapcsol
két oxigénatomot és
szén-dioxid molekula
keletkezik (ábra).
 Ha 1
gramm szén (jele C) atomjai égés közben a levegő oxigén atomjaival szén-dioxid
(CO2) molekulákká egyesülnek, akkor 8 kilogrammkalória, kb. 3400 méterkilogrammsúly
munkavégző képesség szabadul fel
Ha 1
gramm szén (jele C) atomjai égés közben a levegő oxigén atomjaival szén-dioxid
(CO2) molekulákká egyesülnek, akkor 8 kilogrammkalória, kb. 3400 méterkilogrammsúly
munkavégző képesség szabadul fel
De mit jelent elképzelhetően az, hogy ilyenkor meleg keletkezik? Hiszen eddig azt mondtuk, hagy a hőfejlődés az anyag részecskéinek sebesebb mozgását jelenti. Ha az a szénatom két oxigénatommal új molekulát alkot (bekövetkezik az égés), akkor miért kezdenek nagyobb sebességgel mozogni a szomszédos levegőmolekulák? Miért kíséri a kémiai egyesülést a láng, a fény?
A sasmadarak és a kémiai egyesülés
Előre is elnézést kérek, ha egy túlságosan szemléletes példát mondok, de ez
jól megmagyarázza a dolgot.
Egyesülés előtt azok az oxigén- és szénatomok vagy molekulák békésen végezték a maguk mindennapi hőmozgását, szálldostak ide-oda, közben összeütköztek más
részecskékkel, de visszapattantak és tovább repültek.
Képzeljünk a szénatom
helyébe egy rétisas-madarat, az oxigénatomok
helyébe pedig egy-egy saskeselyűt. - Ezek a madarak is békésen szállnak ide-oda,
végzik a maguk mindennapi röpködését.
De egyszer csak egymáshoz közel kerülnek, és a sasok lábai hirtelen egymáshoz
láncolódnak erős és rövid lánccal, hasonlóan ahhoz, amiként a kémiai erők egymáshoz
láncolják az atomokat.
Mi történik a sasokkal a következő pillanatban?
Kétségbeesett csapkodással igyekeznek szabadulni. Hol ide, hol oda röppenek,
vadul keringenek - igazán nem lenne ajánlatos a közelükbe kerülni. De ha más
madarak mégis odakerülnek, azokat csapkodásuk közben úgy meglökhetik, hogy messzire
lódulnak.
Így lehet elképzelni az atomok egymáshoz láncolását, kémiai egyesülését is.
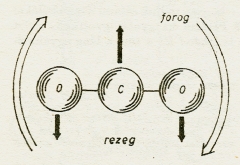 A szén-dioxid
molekulában egymáshoz láncolt atomok heves, ide-oda történő rezgő mozgást végeznek,
sőt még vadul körbe is forog az egész molekula (ábra).
A szén-dioxid
molekulában egymáshoz láncolt atomok heves, ide-oda történő rezgő mozgást végeznek,
sőt még vadul körbe is forog az egész molekula (ábra).
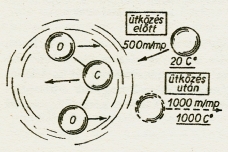 Ha a
hevesen mozgó. Szén-dioxid molekula úgy meglöki a 20°C hőmérsékletű szobalevegőben
békésen szálló nitrogénatomot, hogy ennek sebessége kétszer akkora lesz, mint
előbb volt, akkor ennek a sebességnek kb. 1200°C hőmérséklet felel meg (pontosabban1172°C)
Ha a
hevesen mozgó. Szén-dioxid molekula úgy meglöki a 20°C hőmérsékletű szobalevegőben
békésen szálló nitrogénatomot, hogy ennek sebessége kétszer akkora lesz, mint
előbb volt, akkor ennek a sebességnek kb. 1200°C hőmérséklet felel meg (pontosabban1172°C)
Tegyük fel, hogy egy békésen szálldogáló levegőmolekula kerül a hevesen rángatódzó,
őrülten forgó szén-dioxid molekula mellé. Ez a levegőmolekula olyan lökést kaphat,
hogy sebessége kétszeresre is nőhet (ábra). Olyan erejű lökést kaphat,
hogy a lökés energiája elegendő ahhoz, hogy a levegőmolekulát fénykibocsátásra
gerjessze.
A lökés folytán nagy sebességet
nyert levegőmolekulák természetesen meglökdösik a környezetükben levő többi
levegőmolekulát. A levegő minden irányban felmelegszik. Lehet, hogy az ütközés
még mindig olyan erős, hogy fénykibocsátással
jár.
Íme, így keletkezik a fény, a láng az oxigénnel egyesülő szénatomok közelében.
Így terjed a meleg a kémiai egyesülés helyéről.
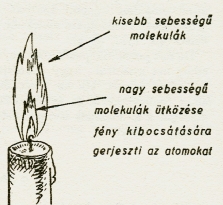 Az is azonnal
belátható, hogy a lökdösés ereje az egyesülés helyétől távolabb egyre csökken,
hiszen az először meglökött levegőrészecske energiája egyre több részecske között
oszlik el. Egyszer csak nem lesz olyan erős az ütközés, hogy fényt gerjesszen.
Itt lesz a láng határa (ábra).
Az is azonnal
belátható, hogy a lökdösés ereje az egyesülés helyétől távolabb egyre csökken,
hiszen az először meglökött levegőrészecske energiája egyre több részecske között
oszlik el. Egyszer csak nem lesz olyan erős az ütközés, hogy fényt gerjesszen.
Itt lesz a láng határa (ábra).
Miért van a lángnak határa? - Mert a molekulák sebessége az egyesülés helyétől távolabb egyre csökken
Így lesz tehát a kémiai egyesülésből fizikai mozgás, Így fejlődik hő, fény,
láng.
Miért hidrogén ég a rakétamotorban?
Ma az emberiség legfontosabb energiaforrása az égés. Elektromos erőműveinkben, járműveink motorjaiban, a rakéták hajtóműveiben különféle anyagok égnek el (egyesülnek oxigénnel). Mennél több hő szabadul fel 1 kilogramm anyag elégésekor, annál több felhasználható energiához jutunk.
 Ha egy esetben 1 kg szalmát égetünk el a vizesüst alatt, máskor meg 1 kg kőszenet,
akkor ugyanaz a vízmennyiség nem egyenlő mértékben melegszik fel, mert 1 kg
szalma elégésekor kevesebb meleg keletkezik, mint 1 kg kőszén elégésekor.
Ha egy esetben 1 kg szalmát égetünk el a vizesüst alatt, máskor meg 1 kg kőszenet,
akkor ugyanaz a vízmennyiség nem egyenlő mértékben melegszik fel, mert 1 kg
szalma elégésekor kevesebb meleg keletkezik, mint 1 kg kőszén elégésekor.
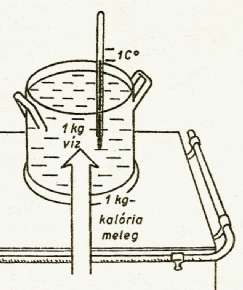
Ha 1 kg vizet addig melegítünk, amíg hőmérséklete 1°-kal emelkedik, akkor azt
mondjuk, hogy a vízbe 1 kilogrammkalória mennyiségű hőt juttatunk (ábra).
Ha 1 kg víz hőmérséklete 1°C-kal emelkedik melegítés közben, akkor a víz 1 kilograrmmkalória (1 kcal) hőmennyiséget vesz fel
Egy kilogrammkalória tehát az a hőmennyiség, amely 1 kg víz hőmérsékletét 1°-kal emeli. Jele: kcal.
Tüzelőszereink jóságát úgy állapíthatjuk meg, hogy a különböző tüzelőszerekből
1 kg-ot elégetünk és
megmérjük (pl. a víz felmelegedéséből),
hogy hány kalória
keletkezik.
1 kg anyag elégésekor
felszabaduló meleg
kilogrammkalóriákban
kifejezve
| Puskapor |
800
|
| Dinamit |
1300
|
| Barnaszén |
3000
|
| Szalma |
3600
|
| Kukoricacsutka |
3700
|
| Fa |
4500
|
| Spiritusz |
6400
|
| Kőszén (legjobb) |
7000
|
| Petróleum, benzin |
10000
|
| Hidrogén |
34000
|
Sok érdekeset mond ez a táblázat. Például ki hitte volna, hogyha a szalmát olyan gyorsan sikerülne elégetni, mint a dinamitot, akkor majdnem háromszor hatásosabb robbanóanyag lenne a szalma és a kukoricacsutka, mint a dinamit.
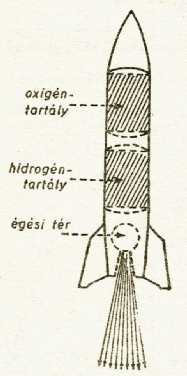 A táblázatból
látjuk, hogy a hidrogén égésekor szabadul fel legtöbb hő, legtöbb energia. Ha
tehát a rakétát építő mérnök azt akarja) hogy a rakéta a lehető legtöbb hajtóenergiát
adó üzemanyagot vigyen magával, akkor a rakéta egyik üzemanyagtartályát hidrogénnel,
a másikat pedig oxigénnel tölti meg (ábra).
A táblázatból
látjuk, hogy a hidrogén égésekor szabadul fel legtöbb hő, legtöbb energia. Ha
tehát a rakétát építő mérnök azt akarja) hogy a rakéta a lehető legtöbb hajtóenergiát
adó üzemanyagot vigyen magával, akkor a rakéta egyik üzemanyagtartályát hidrogénnel,
a másikat pedig oxigénnel tölti meg (ábra).
A rakéta az égéshez szükséges oxigént is magával viszi. A másik tartályban olyan üzemanyag van amelynek égési hője nagy
De egy kis baj van! A hidrogén
is, az oxigén is gáz
alakban fordul elő. Néhány tízezer kilogramm ilyen gáz
szükséges az űrrakéta hajtására. Óriási gáztartályokat kellene magával vinnie
a rakétának. Lehetetlen tehát gáznemű hidrogént
és oxigént alkalmazni.
Cseppfolyósítani kell őket, hogy cseppfolyós,
kisebb térfogatú állapotban vigye magával a rakéta.
Igen ám, de a hidrogént
-240°C fokra kell lehűteni, hogy cseppfolyósodjék, és ekkor gőzének
nyomása 13 légköri
nyomás.
Az oxigént pedig -119°C
fokra kell lehűteni, hagy cseppfolyósodjék, és gőze ekkor 51 atmoszféra nyomással
feszíti a tartályt!
Mindez óriási nehézséget jelent a rakétaépítőknek. Ha ezt tudjuk, még jobban
megbecsüljük az elért sikereket.